The Telegraph berichteten kürzlich, dass der Öffentlichkeit gesagt wurde, sie solle die Einnahme von Husten- und Erkältungsmitteln wegen Sicherheitsbedenken in Bezug auf das Medikament Pholcodin, ein Opioid-Hustenstiller, einstellen.
Zwanzig der gebräuchlichen Husten- und Erkältungsmedikamente, darunter die Kapseln der Tages- und Nachtpflege, wurden auf Anordnung der Arzneimittelbehörden dringend vom Markt genommen, da Bedenken hinsichtlich eines „sehr seltenen“ Risikos einer Anaphylaxie, einer lebensbedrohlichen Nebenwirkung, bestehen.
Die Ankündigung des Rückrufs von Arzneimitteln der Klasse 2 stammt von der britischen Regierung Website wird unten gezeigt.

Bei den mRNA-COVID-19-Impfstoffen war die regulatorische Doppelmoral noch nie so offensichtlich.
Anaphylaxie wurde von der Europäischen Arzneimittelagentur bereits im Dezember 2020 im CHMP (Committee for Medicinal Products for Human Use) der EMA als bedeutendes Risiko identifiziert Beurteilung zum Pfizer-BioNTech COVID-19-Impfstoff, siehe unten.
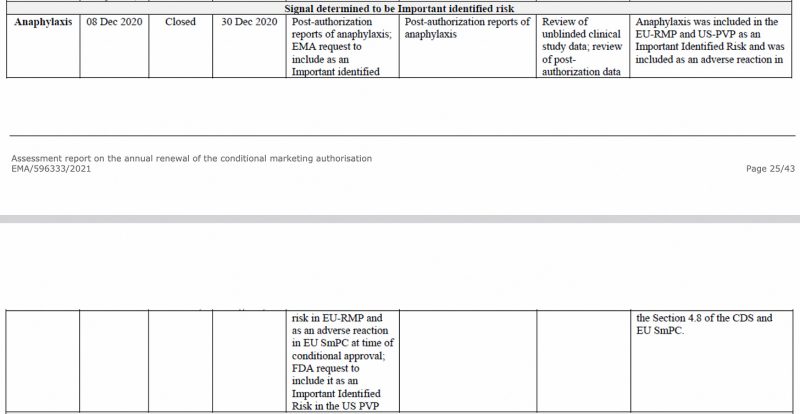
Auch im ersten regelmäßigen Sicherheitsupdate der EU Profil melden, die ich vorher hatte analysiertwurde Anaphylaxie erneut als wichtiges identifiziertes Risiko gekennzeichnet.

In diesem Pharmakovigilanzbericht wurden aus den Daten nach der Zulassung 3,827 relevante Fälle (Einzelpersonen) identifiziert. Das Land mit der höchsten Inzidenz war Japan, gefolgt von den USA und Großbritannien.
Die höchste Anzahl gemeldeter Fälle wurde bei Frauen verzeichnet, schockierende 3,182 Fälle im Vergleich zu 454 Fällen bei Männern mit einem Durchschnittsalter von 44 Jahren. Die Tatsache, dass siebenmal mehr Fälle bei Frauen gemeldet wurden, ist nichts Neues. Bereits im Dezember 7 habe ich analysiert der Pfizer vorbereitet Dokument für die FDA, die den 3-Monats-Zeitraum von Dezember 2020 bis 28. Februar 2021 abdeckt – im Fall von Anaphylaxie waren Frauen 8-mal häufiger betroffen.
Damit wurden 98 Prozent der relevanten unerwünschten Ereignisse (darunter anaphylaktische Reaktion, anaphylaktischer Schock, anaphylaktoide Reaktion und anaphylaktoider Schock) als schwerwiegend eingestuft!
Darüber hinaus betrug bei 92 Prozent der Ereignisse die verstrichene Zeit bis zum Auftreten eines unerwünschten Ereignisses nach der Impfstoffverabreichung weniger als 24 Stunden.

Tödliche Folgen
Von den 3,922 Ereignissen waren 28 tödlich und bei erstaunlichen 704 war der Ausgang unbekannt. Für Todesfälle wurden keine Fallzahlen angegeben.

Fälle nach Altersgruppen
Von den 3,827 relevanten Fällen (Einzelpersonen) stammten 23 aus der Altersgruppe der Kinder und 3,021 aus der Altersgruppe der Erwachsenen.
Vorhandensein von Komorbiditäten
Bemerkenswert ist, dass dies bei etwa 2/3 aller Anaphylaxiefälle der Fall war nicht Komorbiditäten (zugrunde liegende Gesundheitsprobleme) haben.

Angesichts dessen, was seit der Einführung der mRNA-COVID-19-Impfstoffe geschehen ist, überrascht es nicht, zu lesen: „es wurden keine neuen Sicherheitsinformationen identifiziert zum Risiko einer Anaphylaxie mit BNT162b2“ (Pfizer-BioNTech COVID-19-Impfstoff). Der angegebene Grund (oder die Entschuldigung, hinter der sie sich verstecken) ist, dass „dieses Risiko kommuniziert wird im Falle eines seltenen anaphylaktischen Ereignisses nach Verabreichung des Impfstoffs.“
Der Regel 174, Informationen für Angehörige der Gesundheitsberufe im Vereinigten Königreich, das zuletzt im Dezember 2021 überarbeitet wurde, heißt es:

n in der Tat, ganz im Gegenteil erster Tag der Einführung des COVID-19-Impfstoffs von Pfizer-BioNTech in Großbritannien gab es zwei Berichte über Anaphylaxie und einen gemeldeten Fall einer möglichen allergischen Reaktion. Dies hinderte die MHRA nicht daran, das Produkt zurückzurufen – sie umgingen das Problem einfach, indem sie erklärten, dass Menschen mit einer Vorgeschichte von Allergien den Impfstoff nicht einnehmen sollten.
Selbst als sie wussten, dass Pfizer/BioNTechs Lipid-Nanopartikel-Inhaltsstoffe ALC-0159 und ALC-0315 noch nie in einem zugelassenen Medikament enthalten waren. ALC-0159 enthält PEG (Polyethylenglykol), das ist bekanntermaßen Anaphylaxie verursachen.
Es ist eindeutig: Anaphylaxie war ein bekanntes lebensbedrohliches unerwünschtes Ereignis, etwa zur gleichen Zeit, als die Notfallzulassung für den COVID-19-Impfstoff von Pfizer-BioNTech erteilt wurde. Da es sich jedoch um einen „injizierbaren Impfstoff“ handelt, hat es irgendwie einen Freibrief von allen Arzneimittelbehörden erhalten, egal wie viele vernichtende Daten sich ansammeln, wenn ein Hustensaft oder eine Kapsel andererseits aufgrund eines „a sehr seltenes Anaphylaxierisiko.“
Wiederveröffentlicht von der Autorin Substack
Veröffentlicht unter a Creative Commons Namensnennung 4.0 Internationale Lizenz
Für Nachdrucke setzen Sie bitte den kanonischen Link wieder auf das Original zurück Brownstone-Institut Artikel und Autor.









